Bilangan Kuantum
A.PENDAHULUAN
Bilangan kuantum adalah suatu harga yang menyatakan keadaan orbital suatu atom.
Bilangan kuantum terdiri dari:
1) Bilangan kuantum utama(n), menyatakan tingkat energi/kulit atom.
2) Bilangan kuantum azimuth(l), menyatakan sub-kulit atom dan bentuk geometri orbital
3) Bilangan kuantum magnetik(m), yaitu menyatakan banyak dan posisi/orientasiorbital
4) Bilangan kuantum spin(s), menyatakan kedudukan elektron dalam suatu orbital.
- Bilangan kuantum utama/prinsipal(n) adalah suatu harga yang menyatakan tingkatenergi atau kulit dalam atom.
- Bilangan kuantum utamamerupakan dasar penentu harga bilangan kuantum lainnya.
- Bilangan kuantum utama antara lain:
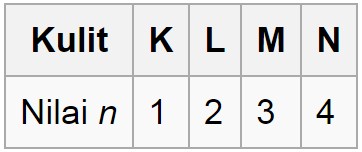
C.BILANGAN KUANTUM AZIMUTH
- Bilangan kuantum azimuth/orbital(l) adalah suatu harga yang menyatakan sub-kulit atom dan bentuk geometri orbital.
- Harga l yang diijinkan di setiap kulitnya adalah:
- Kulit-kulit atom dalam keadaan penuh terisi elektron beserta harga b.k.azimuth:
D.BILANGAN KUANTUM MAGNETIK
- Bilangan kuantum magnetik(mlatau m) adalah suatu harga yang menyatakan banyak dan posisi/orientasi orbital.
- Harga m yang diijinkan di setiap sub-kulitnya: -l ≤ m ≤ +l
- Posisi/orientasi atau orbital adalah tempat dimana elektron bergerak didalam atom, dan masing-masing orbital maksimal menampung sepasang elektron.
- Sub-kulit atom dalam keadaan terisi penuh elektron beserta harga b.k. magnetik:
E.BILANGAN KUANTUM SPIN
- Bilangan kuantum spin (msatau s) adalah suatu harga yang menyatakan kedudukan dan arah rotasi elektron pada suatu orbital.
- Bilangan kuantum spin tidak digunakan dalam menentukan keadaan orbital, hanya untuk menentukan perbedaan elektron pada orbital.
- Karena terdapat dua elektron dalam satu orbital, sedangkan keduanya memiliki kutub padanya, maka nilai elektron yang berpasangan dalam orbital tersebut harus berbeda nilai.
- Harga bilangan kuantum spin terdiri dari:
F.BENTUK ORBITAL
- Bentuk orbital bergantung pada harga bilangan kuantum azimuth (l), dan setiap nilai lmemiliki bentuk orbital berbeda.
- Orbital p berbentuk satu buah balon yang dipilin atau dua bola
- Orbital d berbentuk dua buah balon yang dipilin atau empat bola .
- Orbital f berbentuk empat buah balon yang dipilih atau delapan bola.
- Hibridisasi adalah gabungan orbital-orbital atom dalam suatu senyawa membentuk orbital hibridmolekul. (lihat di bagian Bentuk dan Interaksi Molekul)
G.DIAGRAM ORBITAL
- Diagram orbital menggambarkan urutan konfigurasi elektron dalam setiap kulit atom.
- Konfigurasi elektron yang ditulis menggunakan bilangan kuantum harus memenuhi kaidah berikut.
1) Azas Aufbau
Aturan pengisian sub-kulit:
Contoh:
8O : 1s22s22p41
9K : 1s22s22p63s23p64s1
26Fe : 1s22s22p63s23p64s23d8
2) Aturan Hund
- Penyimpangan pengisian sub-kulit terjadi pada sub-kulit d, karena menginginkan kestabilan.
- Sub-kulit d stabil apabila terisi 5 atau 10 elektron, sehingga apabila terdapat 4 atau 9 elektron pada sub-kulit d, maka sub-kulit d akan ‘meminjam’ elektron dari sub-kulit s.
- Sub-kulit d juga mengalami penyimpangan pada unsur-unsur lantanida dan aktinida, dimana sebelum mengisi sub-kulit f, terdapat satu elektron yang mengisi sub-kulit d terlebih dahulu.
3) Larangan Pauli
- Penulisan konfigurasi elektron dapat dipersingkat dengan menggunakan notasi gas mulia.
H.GOLONGAN DAN PERIODE PADA TABEL PERIODIK
- Konfigurasi elektron dengan diagram orbital dapat digunakan untuk menentukan blok, golongan, dan periode unsur dalam sistem periodik modern.
- Blok unsur merupakan pembagian unsur berdasarkan sub-kulit terakhir yang diisi oleh suatu atom.
- Penentuan golongan dan periode unsur pada tabel periodik utama adalah sebagai berikut.
- Penentuan golongan dan periode unsur pada tabel periodik unsur lantanida dan aktinida:
- Unsur-unsur lantanida merupakan blok f dengan konfigurasi 6s2 5d1 4f1 s.d.14.
- Unsur-unsur aktinida merupakan blok f dengan konfigurasi 7s2 6d1 5f1 s.d.1
